Иммунореабилитация детей с рекуррентными респираторными заболеваниями
Автор: Мырзабекова Г.Т., Рахметилдаева Г.М. Дата: 13.05.2018 Просмотров: 1227 Комментарии: 0

Современные возможности иммунореабилитации детей с рекуррентными респираторными заболеваниями
Аннотация
Проблема иммунореабилитации детей с рекуррентыми (повторными) респираторными заболеваниями, несмотря на большое число исследований, остается до конца нерешенной. Предложены возможности повышения иммунитета и профилактики частых респираторных заболеваний у данной группы детей.
Аннотация
Рекуррентік (қайталама) респираторлық ауруға шалдыққан балалардың иммунореабилитация мәселесі зерттеу санының көптігіне қарамастан, бүгінгі күнге дейін өз шешімін таппауда. Бұл мақалада берілген балалалар тобындағы жиі кездесетін респираторлық сырқаттарды алдын алу және иммунитетті көтерудің мүмкіншіліктері ұсынылды.
Summary
Despite the large number of studies, the problem of children’s immunorehabilitation with recurrent (repeated) respiratory diseases remain unresolved. Offered opportunities to boost immunity and prevent frequent respiratory diseases in this group of children.
Ключевые слова: часто болеющие дети, имунореабилитация, эффективность
Мырзабекова Г.Т., Рахметилдаева Г.М.
КазМУНО, кафедра педиатрии с курсом детской онкологии и гематологии
Полученные в последние годы данные свидетельствуют о том, что иммунная система часто болеющих детей (ЧБД) хотя и не имеет грубых первичных и приобретенных дефектов, но характеризуется крайней напряженностью процессов иммунного реагирования, нарушением межклеточной кооперации и недостаточностью резервных возможностей, что, по-видимому, является результатом длительного и массивного антигенного воздействия на организм ребенка. Рекуррентными респираторные заболевания (РРЗ) – это не нозологическая форма и не диагноз, возникающие из-за транзиторных корригируемых отклонений в защитных системах организма и не имеющих стойких органических нарушений в них. Повышенная восприимчивость к респираторным инфекциям у таких детей не связана со стойкими врожденными и наследственными патологическими состояниями. При рекуррентных респираторных заболеваниях: нарушается функционирование различных органов и систем, снижается иммунорезистентность организма и наблюдается срыв компенсаторно-адаптивных механизмов; изменяется режим двигательной активности, что способствует развитию фоновых заболеваний (рахит, дистрофия, анемия и др.) и отставанию в физическом и психомоторном развитии; неоправданно используется большое количество медикаментов (полипрагмазия), в том числе салицилаты и антибиотики, которые обладают иммунносупресивным действием; нарушается социальная адаптация контактов со сверстниками.
Исследования [1] показали, что у детей с рекуррентными респираторными заболеваниями даже в период клинического благополучия и при отсутствии признаков ОРЗ выявляются отчетливые изменения в межклеточном взаимодействии в иммунной системе: достоверно повышено содержание провоспалительных интерлейкинов (IL2, IL4), в том числе интерлейкинов, участвующих в хронизации процессов воспаления (IL6, IL8). Это сопровождается снижением клеточной цитотоксичности, дисиммуноглобулинемией и повышением уровня клеток, экспрессирующих рецепторы, индуцирующие апоптоз. При этом индуцированная продукция провоспалительных цитокинов была недостаточной, что свидетельствует об истощении резервных возможностей иммунной системы организма ребенка. Снижение количества CD11b клеток, в состав которых входят гранулоциты, моноциты, натуральные киллеры и макрофаги, экспрессирующие молекулы межклеточной адгезии, а также уменьшение количества эндотелиальных клеток, экспрессирующих межклеточные молекулы адгезии 1-го типа и рецепторы к риновирусам, во многом объясняют повышение чувствительности детей к повторным респираторным вирусным инфекциям и склонность их к развитию бактериальных осложнений. А недостаточность резервных возможностей интерфероногенеза, особенно в плане синтеза γ-интерферона, осуществляющего мощную противовирусную защиту в организме, несмотря на нормальный уровень интерферона в сыворотке крови, объясняет сохранение вялотекущей реакции воспаления в организме ребенка даже при отсутствии клинических признаков ОРЗ [1]. В связи с этим представляет интерес препараты, позитивно влияющие на иммунологический показатели.
Бета-глюканы — это крупные молекулы, не подвергающиеся ферментативной фрагментации в желудочно-кишечном тракте. Они захватываются клетками слизистой оболочки кишечника и активно переносятся в подслизистый слой, где активируют макрофаги, а через них — лимфоциты, ответственные за защиту эндотелия, то есть за местный иммунитет [3]. Благодаря механизму репопуляции активированные лимфоциты из слизистой оболочки кишечника диссеминируют в слизистые оболочки различных органов, обеспечивая, таким образом, их защиту от инфекций [2]. Механизм действия бета1,3/1,6глюкана в целом можно объяснить его выраженной селективностью в отношении специфических рецепторов на поверхности макрофагов, связывающихся только с неразветвленным участком молекулы бета-глюкана, в результате чего происходит активация макрофагов, что приводит к реализации триггерных механизмов целого ряда процессов, направленных на иммунную защиту организма [3]. С одной стороны, активируется фагоцитарная функция макрофагов, с другой — начинают усиленно синтезироваться и высвобождаться такие вещества, как цитокины (интерлейкины, интерферон), являющиеся сигналом для других клеток иммунной системы, например Т-лимфоцитов, фактора роста эпидермальных клеток, фактора ангиогенеза [6]. Бета-глюканы активируют как местный иммунитет, обеспечивая защиту организма от вторжений антигенов, так и системный иммунитет, что приводит к уничтожению уже проникшего внутрь организма чужеродного генетического материала и восстановлению иммунного гомеостаза. При этом следует подчеркнуть отличительную особенность иммуномодулирующего действия бета1,3/1,6-глюкана, которая состоит в адекватном повышении активности иммунной системы без ее чрез мерной стимуляции, что нередко служит причиной возникновения аутоиммунных заболеваний.
Цель нашего исследования - оценка клинико-иммунологической эффективности сиропа Бета-Глюкан 100 мл у детей с рекуррентными респираторными заболеваниями. Дизайн исследования представляло проспективное, открытое, контролируемое клиническое исследование терапевтической эффективности и безопасности применения препарата. В исследование были включены 30 детей обоего пола от 1 года до 7 лет, имеющие рекуррентные респираторные заболевания на фоне, аллергических заболеваний и нарушения нормального микробиоценоза кишечника.
Детям от 1года по 5 мл (1 ч.л.) один раз в день утром натощак за 30 минут до еды, детям от 3 лет по 15 мл (1 стол.л.) один раз в день за 30 мин до еды. Продолжительность наблюдения составила 1 месяц.
Критериями оценки эффективности определили: положительная клиническая динамика и показатели иммунограммы (клеточный и гуморальный иммунитет). Также детям проводили физикальный осмотр детей во время скрининг-визита и контрольных визитов, лабораторные данные (общеклинические и биохимические критерии).
Программа клинической апробации терапевтической эффективности и безопасности применения сиропа Бета-глюкан 100 мл была рассмотрена и одобрена на заседании этического комитета при Академии питания Республики Казахстан №5 от 04.04.16 г.
Было получено письменное согласие каждого родителя\опекуна ребенка на основе предоставления полной информации об исследовании. Все испытуемые были ознакомлены со своими правами, получили «Информационный лист испытуемого», подписали «Информированное согласие испытуемого». Цель исследования, процедуры протокола и потенциальный риск были разъяснены участникам понятным языком, без использования специальной терминологии. Перед вовлечением в исследование родителям\опекунам детей было необходимо прочитать и подписать форму информированного согласия, за ними было оставлено право отказаться от участия в исследовании в любой момент, не рискуя остаться без медицинской помощи. Участникам выданы копии их форм информированного согласия.
В исследование были включены дети по следующим критериям:
1. Частота эпизодов ОРВИ в год
Критерии включения детей в группу РРЗ (В.Ю. Альбицкий, А.А. Баранов, 1986 г.):
| Возраст детей | Частота ОРВИ (эпизодов/год) |
| 1-го года жизни | 4 и более |
| До 3-х лет | 6 и более |
| 4-5 лет | 5 и более |
| Старше 5 лет | 4 и более |
2. Нарушение в иммунограмме ребенка: дефекты гуморального и/или клеточного звена иммунитета.
3. Нарушение нормального микробиоценоза кишечника у детей, проявляющиеся: неустойчивым стулом, кишечными коликами, болями в животе, метеоризмом, неприятным запахом изо рта и снижением аппетита.
4.Согласие родителей и/или опекунов на участие ребенка в клинической апробации.
Критерий исключения:
- Возраст младше года и старше 7 лет;
- Онкологические заболевания;
- Клинически значимые заболевания печени (например повышение уровня аланинаминотрансферазы и / или аспартатаминотрансферазы и / или общего билирубина ≥ 5 раз выше верхней границы нормы)
- Хроническая болезнь почек
- Дети с задержкой психо-физического развития;
- Дети с сахарным диабетом 2 типа;
- Воспитанники детских домов, интернатов;
- Повышенная чувствительность к компонентам БАД.
Всем пациентам будут проводиться следующие методы исследования:
- Сбор анамнеза и общеклиническое обследование (при каждом визите);
- Иммунологическое обследование (иммунограмма крови при каждом визите)
Средний возраст пациентов представлен в таблице 1.
| Пол | Мальчики | Девочки |
| Средний возраст | 13 | 17 |
| 3 | 4,3 |
Как видно из представленных выше данных соотношение по полу и по возрасту в основной группе было однородным. Нозологическая структура была представлена: рекуррентными респираторными заболеваниями на фоне аллергических заболеваний и целиакии у 6,7% детей.
В таблице 2 представлена динамика показателей клеточного и гуморального иммунитета.
Таблица 2. Динамика показателей иммунограммы во время скринингаи по окончании апробации
| Показатель (норма у детей) | Основная группа (n=30) | |
| При первом обращении | 30 дней | |
| Т-Лимфоциты, % (62-69) | 65±3,4 | 64,04±4,1 |
| СD3+, % (21-28) | 23,2±2,4 | 25,8±1,8 |
| СD4+, % (30-40) | 31,2±4,3 | 31,9±4,4 |
| СD8+, % (25-32) | 26,4±2,7 | 27,2±2,1 |
| ИРИ (иммунорегуляторный индекс-1-1,6) | 1,32±0,3 | 1,4±0,1 |
| NK (Натуральные киллеры,%-8-15) | 11,8±3,1 | 11,6±2,2 |
| Фагоцитарный индекс (1,4-2,5) | 1,4±0,2 | 1,6±0,2 |
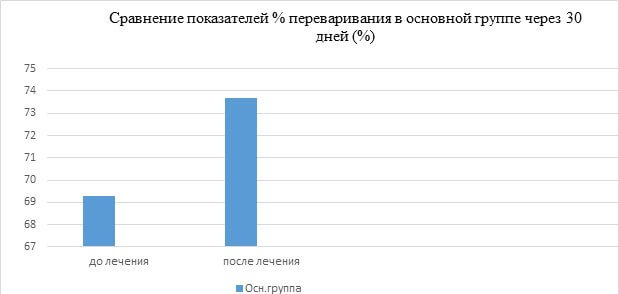
| % переваривания (70-90) | 69,3±3,1 | 73,7±3,7 |
Как видно из таблицы, улучшение показателей иммунограммы происходит в основной группе после проведенной терапии. В особенности, это касается таких показателей иммунограммы как:
- СD3+ (парный t-критерий Стьюдента равен 2.345, критическое значение t-критерия Стьюдента при данном числе степеней свободы составляет 2.06; tнабл >t крит, изменения признака статистически значимы (p<0,05).
- СD8+ (парный t-критерий Стьюдента равен 2.470, критическое значение t-критерия Стьюдента при данном числе степеней свободы составляет 2.06; tнабл>tкрит, изменения признака статистически значимы (p<0,05).
- фагоцитарный индекс (парный t-критерий Стьюдента равен 6.615, критическое значение t-критерия Стьюдента при данном числе степеней свободы составляет 2.045; tнабл>tкрит, изменения признака статистически значимы (p<0,05).
% переваривания (парный t-критерий Стьюдента равен 5.647, критическое значение t-критерия Стьюдента при данном числе степеней свободы составляет 2.045; tнабл>tкрит, изменения признака статистически значимы (p<0,05).
По ниже приведенным показателя иммунограммы статистически значимых изменений выявлено не было:
Т-Лимфоциты - изменения признака статистически не значимы (p>0,05).
СD4+ - изменения признака статистически не значимы (p>0,05).
ИРИ- изменения признака статистически не значимы (p>0,05).
NK - изменения признака статистически не значимы (p>0,05).
На основании динамики показателей иммунограммы можно сделать вывод, что сироп Б-глюкан оказывает положительное иммуномодулирующее влияние на фагоцитарное звено иммунитета, гуморальный иммунитет и в меньшей степени на клеточное звено иммунитета.
Также динамика показателей иммунограммы у пациентов основной группы по окончанию исследования представлена на диаграммах 1 - 4.
Диаграмма 1.
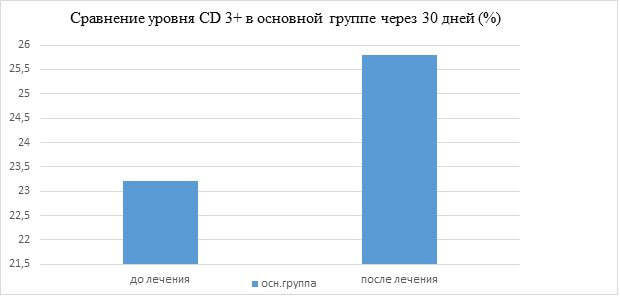
Диаграмма 2.
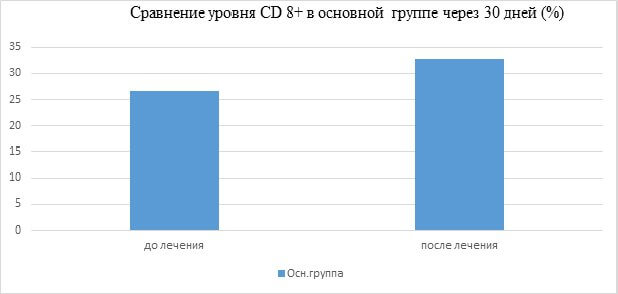
Диаграмма 3.
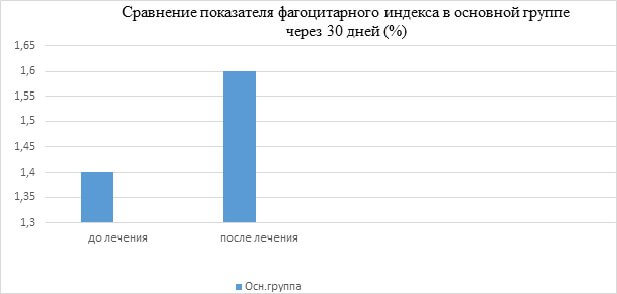
Диаграмма 4.
Данные общего анализа крови пациентов во время скрининга и по прошествии месяца приема сиропа Б-глюкана представлены в таблице 4, а также в диаграммах 5 – 8.
Таблица 3. Динамика общего анализа крови у пациентов основной группы
| № | Показатели общего анализа крови | Основная группа (n=30) | |
| До лечения | После лечения | ||
| 1. | Гемоглобин (г\л) | 122±1,4 | 125,2±1,3 |
| 2. | Эритроциты (*〖10〗^12 г\л) | 4,2±0,1 | 4,7±0,1 |
| 3. | Лейкоциты (*〖10〗^(9 ) г\л) | 5,7±0,4 | 4,9±0.3 |
| 4. | СОЭ (мм\ч) | 5,7±0,8 | 5,2±0,5 |
Приведенные данные показывают, что все гематологические показатели через месяц приема сиропа Б-глюкана находились в пределах нормы. Причем, показатели гемопоэза: эритроциты и гемоглобин после лечения имели статистически значимую положительную динамику (парный t-критерий Стьюдента равен 2.345, критическое значение t-критерия Стьюдента при данном числе степеней свободы составляет 2.06; tнабл>tкрит, изменения признака статистически значимы (p<0,05).
Это косвенно, может доказывать положительное влияние сиропа Бета-глюкан на систему гемопоэза.
Динамика мониторинга биохимических показателей крови у пациентов основной группы во время скрининга и через месяц приема сиропа Б-глюкана представлена в таблице 4.
Таблица 4. Динамика показателей биохимического исследования крови у пациентов основной группы
| № | Показатели биохимического анализа крови | Основная группа (n=20) | |
| До лечения | После лечения | ||
| 1. | АЛТ (ммоль\л) | 24,04±3,35 | 23,68±0,9 |
| 2. | АСТ (ммоль\л) | 23,16±2,54 | 23,36±3,6 |
При анализе данных биохимического анализа крови (АЛТ,АСТ) не отмечено гепатоксического действия Бета Глюкана.
Таким образом, детский сироп Б-глюкан (100 мл) обладает удовлетворительной переносимостью, оказывает иммуномодулирующее действие у детей с рекуррентными респираторными заболеваниями, что может положительно влиять на прогноз дальнейшего течения заболевания, и может быть рекомендован в качестве компонента комплексной терапии при рекуррентных респираторных заболеваниях.
ВЫВОДЫ
1.Применение детского сиропа Б-глюкан (100 мл) оказывает иммуномодулирующее действие на такие показатели иммунограммы как: CD3, CD8, фагоцитарный индекс и % переваривания
2.Статистически достоверная динамика роста гематологических показателей крови при применении Бета-Глюкана в комплексной терапии детей свидетельствует о направленном положительном влиянии продукта на улучшение гемопоэза.
3.Клиническая эффективность Б-глюкан характеризовалась положительным действием: достоверно более быстрое купирование кашля, сокращение продолжительности лихорадки. Профилактическое использование Б-глюкана у обследованных детей позволило при дальнейшем наблюдении за ними снизить частоту заболеваемости ОРВИ в 1,5 раза, уменьшить длительность ее течения у заболевших в среднем на 2 дня, облегчить выраженность симптомов интоксикации, снизить частоту развития бактериальных осложнений, что в конечном итоге позволило также сократить частоту использования у детей антибактериальных препаратов.
СПИСОК ЛИТЕРАТУРЫ
1. 3аплатников А.Л. Клинико-патогенетическое обоснование иммунотерапии и иммунопрофилактики вирусных и бактериальных заболеваний у детей: Автореф. дисс... докт. мед. наук. — М., 2003.].
2. Иммунотропные свойства 1,3/1,6"β"D"глюканов / Беседнова Н. Н., Иванушко Л. А., Звягинцева Т. Н. [и др.] // Антибиотики и химиотерапия. — 2000. — № 2. — С. 37—44.
3. Хаитов P. M. Экологическая иммунология / P. M. Хаитов, Б. В. Пинегин, Х. И. Истамов. — М.,1995. — С. 92—93.
4. Analysis of the sugar specificity and molecular location of the beta"glucan" binding lectin site of complement receptor type 3 (CD11b/CD18) / Thornton B. P., Vetvicka V., Pitman M. [et al.] // J. Immunol. — 1996. — Vol. 156 (3). — P. 1235—1246.
5. Bohn J. A. (1">3)"β"d"Glucans as biological response modifiers: a review of structure"functional activity relationships / J. A. Bohn, J. N. BeMille // Carbohydrate Polymers. — 1995. — Vol. 28 (1). — P. 3—14.
6. Brown G. D. Immune recognition. A new receptor for beta"glucans / G. D. Brown, S. Gordon // Nature. — 2001. — Vol. 413 (6851). — P. 36—37.
7. Dectin"1 is a major beta"glucan receptor on macrophages / Brown G. D., Taylor P. R., Reid D. M. [et al.] // J. Exp. Med. — 2002. — Vol. 196 (3). — P. 407—412.
8. Doll M. Anwendungsbeobachtung: ImmunmodulierendeWirkung von (1,3),(1,6)"β"D"Glucan"Gezeigtan der Neopterin" und b"Defensin" Synthese / M. Doll, R. Hauss, R. Spermezan // Naturheilpraxis. — 2005. — Vol. 5. — P. 676—681.
9. Infection prevention in patients with severe multiple trauma with the immu" nomodulator beta 1—3 polyglucose (glucan) / de Felippe Junior J., da Rocha e Silva Junior M., Maciel F. M. [et al.] // Surg. Gynecol. Obstet. — 1993. — Vol. 177 (4). — P. 383—388. 9. Jesenak M., Hrubisko M. [et al.] // Czech.—Slov. Pediat. — 2010. — Vol. 65 (11). — P. 639—647.
10. Jesenak M., Majtan J. [et al.] // Int. immunopharmacol. — 2013. — Vol. 15 (2). — P. 395—399.
11. Molecular mechanism of tumor necrosis factor"alpha production in 1">3"beta"glucan (zymosan)"activated macrophages / Young S. H., Ye J., Frazer D. G. [et al.] // J. Biol. Chem. — 2001. — Vol. 276 (23). — P. 20781—20787.

